【アボルブカプセル】・・・2015年11月27日、フランスの工場にフランス国立医薬品・医療用品安全管理機構の査察によって、出荷停止になったことが日本国内で報じられました。理由は異物混入のようですが、どのような異物が混入されたのかについて、10日を経過した本日(2015年12月7日)現在詳細が伝えられません。
現在このお薬を服薬中の方は、服薬の是非について主治医の先生の判断を仰いで下さい。
【オルメテック錠】・・・血圧を上げる物質の体内での生成を抑えて、血圧を下げる降圧剤で、日本国内でもかなり使われています。平成25年7月現在、ジェネリックは発売されていませんが、オルメテックと降圧剤であるカルブロックが一緒になったレザルタス配合錠は発売されています。
FDAは、慢性的な下痢・著しい体重減少を引き起こす可能性があると警告を出しました。
原因不明の下痢などに悩んでおられる方は、主治医の先生に相談をしてください。
【イレッサ錠・・・アストラゼネカ社が開発し、2002年に日本が世界で初めて承認した抗がん剤】
当初、イレッサ錠は効果が高く、副作用の少ない画期的な抗がん剤として多くのがん患者に投与されました。
多くの肺がん患者は、高い効果と副作用の少ないことを期待していましたが・・・・後に延命効果は無く、副作用として間質性肺炎(肺繊維症)が認められました。高額な医療費を支払ったうえに、副作用で苦しんでおられる方が日本にもたくさんおられるのです。
〔イレッサ錠 承認から米国市場撤退までの流れ〕
≪2003年≫
米国で、重篤で命を脅かす疾患において市販後に延命効果を証明することを条件として承認された。
↓
≪2005年≫
アストラゼネカ社は、市販後の臨床実験で延命効果を証明できなかったため、 FDA(アメリカ食品医薬品局)は新規患者への投与を禁止し、治療上の利益がある患者以外の使用を著しく制限した。
↓
≪2011年2月1日≫
アストラゼネカ社はイレッサ錠の承認申請を取り下げる予定であることを発表し、これによってイレッサ錠は米国市場から完全に撤退することとなった。
日本では??
日本でも延命効果は証明できていません。
しかし、承認内容が見直される予定もなく、現在再審査を迎えています。
さらに・・・
世界や日本のマスメディアはこのことを報道していません。
※イレッサ錠による治療や服薬に関して不安や質問がある方は、主治医の先生又は、薬剤師に相談してみて下さい。
※イレッサ錠についての情報や被害に遭われた方の近況報告などを知ることができます。→イレッサ薬害被害者の会のホームページへ。
【アクトス錠・・・血糖値を下げる薬です。糖尿病の治療に用います。】
上記の薬剤を長期間使用することにより、膀胱癌発生リスクをわずかに高める可能性があります。
2011年6月15日、米国食品医薬品局(FDA)は、米国の患者さん宛に下記のように発表しました
- ピオグリタゾンを服用する場合には膀胱癌になる可能性が上昇するかもしれない。
- 膀胱癌の治療を受けている場合は、ピオグリタゾンは服用すべきではない。
- 膀胱癌を疑わせる症状(尿が赤くなった場合、急な尿意や排尿痛、背部痛 あるいは下腹部痛)がみられた場合は速やかに医師に連絡すること。
- ピオグリタゾンによる治療に関して質問や不安がある場合は、医療関係者に連絡すること。
- 平成23年6月9日にフランス保健製品衛生安全庁は、ピオグリタゾン製剤について、当面は医師に対する新規処方の差し止め及び、現在服用している患者様においては主治医への相談前に服薬を中止すべきではないことを通達しました。また、6月10日にドイツ連邦医薬品医療機器庁からもフランスと同様の措置が通達されています。
- 現時点で、日本ではピオグリタゾン製剤の服用の中止、あるいは変更は推奨されていません。(2011.7.5)
- アクトス錠にはジェネリック医薬品もあります。他に、アクトス錠を含有する糖尿病治療薬もあります。処方されたお医者さん又は薬剤師さんに、ご自身が服用されている薬がアクトス錠と関係があるか尋ねてみて下さい。
アクトス錠15mg アクトス錠30mg
※アクトス錠を服用している患者様へ
くれぐれもご自身の判断で薬の使用を中止しないで下さい!!必ず、主治医の先生に相談してください。
三共株式会社
藤沢薬品株式会社
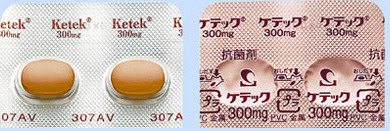
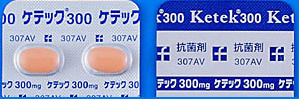
- ケテック錠って何のお薬?
- 抗生物質(細菌の育成を抑えるお薬)です。
- 副作用ってあるの?
- 重篤な副作用が報告されました!!意識消失があらわれることがあります。
ケテック錠による意識消失の副作用が2004年12月28日までに15例報告されています。そのうち4例は自動車事故例が含まれていました。
ケテック錠を服用中には、自動車の運転等、危険を伴う機械の操作は避けてください。
メリロート・・・健康食品の製品名(ヨーロッパや、アジアの温帯地域に分布しているマメ科の植物)
事例1:被験者 20歳代 女性 (静岡県)
- 平成14年1月よりメリロートを摂取した。同時にブルーベリーエキスも摂取した。
- 平成14年5月の健康診断において血液検査でGOT、GPT等の上昇を指摘され(自覚症状無し)、翌日、医療機関に受診し、同日に入院となった。その後、加療により軽快し同年7月に退院した。
- 当該製品以外に薬物や健康食品は摂取しておらず、入院して摂取を中止することにより肝機能の改善がみられたこと、他のウイルス性肝炎等は否定されていることから、当該製品の摂取による肝障害であることが強く疑われた。
事例2:被験者 30歳代 女性 (新潟県)
- 平成13年6月からメリロートを摂取した。
- 平成13年7月、黄疸、倦怠感を訴え受診、翌日に入院した。その後、加療により軽快し同月中に退院したが、再び当該食品を摂取したところ再発し、翌日に再入院した。その後、8月に退院した。
- 他のウイルス性肝炎等は否定されており、当該患者の症状の経過から、当該製品の摂取による肝障害であることが疑われた。
なお、どちらの事例も製品は同一販売者のものです。同一の製品名で複数社が販売していますが報告があったのは特定の1社だけです。
- メリロートの原材料名
- メリロートエキス末、クミスクチンエキス末、イチョウ葉エキス末、トウガラシ抽出物、オリーブ油、ゼラチン、グリセリン、ミツロウ、グリセリン脂肪酸エステル
- ブルーベリーエキスの原材料名
- ブルーベリーエキス末、カロチノイド、ビタミンB1、ビタミンB2、ビタミンB6、ビタミンB12、マリーゴールド、ゼラチン、シソ油、グリセリン、ミツロウ
上記薬剤の併用により、副腎皮質ステロイド剤を全身投与した場合と同様の症状があらわれる可能性があります。
フルナーゼ点鼻液とリトナビルの併用によりクッシング症候群、副腎皮質機能抑制等が報告されているので、リトナビルとの併用は治療上の有益性がこれらの症状発現の危険性を上回ると判断される場合に限ること。

フルナーゼ点鼻液
<クッシング症候群とは?>
臨床症状として、満月様顔貌や野牛肩などがあります。小児では身長の発育停止が特徴的です。女性は通常月経不順となります。
2002年6月の発売以降、上記薬剤との関連性が否定できない重篤な低血糖症例が75例、高血糖症例が14例報告されています。(推定使用者数:420万人、2003年2月末)
2008年9月30日で、販売中止となりました。
副作用の発現症例
- 80歳代 女性:尿路感染症、褥瘡のため投与
合併症:糖尿病、両膝関節症、腰痛症、循環改善、胃炎、めまい、便秘
上記薬剤3日間投与、低血糖を引き起こす。中止後回復。
- 60歳代 男性:尿路感染症のため投与
合併症:糖尿病、うっ血性心不全、高コレステロール血症、高尿酸血症
上記薬剤2日間投与、低血糖を引き起こす。中止後回復。
- 50歳代 女性:尿路感染症のため投与
合併症:糖尿病、精神分裂病、高血圧
上記薬剤4日間投与、低血糖を引き起こす。中止後回復。
- 80歳代 女性:急性気管支炎のため投与
合併症:慢性腎不全、完全房室ブロック(ペースメーカー植え込み後)、憎帽弁閉鎖不全症、慢性心不全、心室性期外収縮
上記薬剤2日間投与、低血糖を引き起こす。中止後回復。
- 60歳代 男性:非定型抗酸菌症のため投与
合併症:糖尿病、骨粗鬆症、肝硬変、肺線維症、浮腫
上記薬剤13日間投与、高血糖を引き起こす。中止後回復。
低血糖、高血糖を発現する多くの症例が糖尿病患者であったことから現在では、糖尿病患者には投与できません。

ガチフロ100mg(抗菌剤)
糖尿病の患者以外にも低血糖、高血糖の報告がされているので上記薬剤を服用中に下記の症状があらわれた場合は、服用を中止し、すみやかに医師の診察を受けてください。
- 低血糖症状:脱力感、空腹感、発汗、動悸、振戦、頭痛、不安、興奮、神経過敏、集中力低下、精神障害、意識障害、痙攣等
- 高血糖症状:口渇、多飲、多尿、頻尿
上記薬剤との因果関係が否定できない劇症肝炎が、1993年発売以来、死亡例5例が報告されています。(推定使用患者数:約24万人)
- 服用を開始して6ヶ月間は月1回、その後も定期的な肝機能検査を受けましょう。
劇症肝炎等の重篤な肝障害は、おもに服薬開始から6ヶ月間以内に発現しています。
服薬開始6ヶ月以後は、定期的に肝機能をチェックしてください。
- 服用中に食欲不振・全身倦怠感等があらわれた場合は、医師の診察を受けて下さい。
副作用として肝障害が発生する場合、これらの症状が初期段階として現れます。





